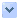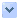亞硫酸鹽與二氧化硫
亞
硫酸鹽 (Sulfites或Sulfiting Agents)
為使用多年之合法食品添加物,不僅是非常有效的酵素抑制劑、漂白劑、抗氧化劑、還原劑及防腐劑,且價格便宜。亞硫酸鹽最早被使用之紀錄是在羅馬帝國時代,
當時是被用於葡萄酒容器之消毒殺菌。此外,許多食品均含有天然存在之亞硫酸鹽,尤其是在各種醱酵食品中。亞硫酸鹽具有殺菌功效及強還原力,可將食品的著色
物還原漂白,並可抑制氧化作用,防止酵素與非酵素褐變反應。合法添加於食品之亞硫酸鹽包括:亞硫酸鈉 (Sodium Sulfite,
Na2SO3)、亞硫酸鉀 (Potassium Sulfite, K2SO3)、亞硫酸氫鈉 (Sodium Bisulfite,
NaHSO3)、亞硫酸氫鉀 (Potassium Bisulfite, KHSO3)、偏重亞硫酸氫鈉 (Sodium
Metabisulfite, Na2S2O5)、偏重亞硫酸氫鉀 (Potassium Metabisulfite, K2S2O5)、低亞硫酸鈉
(Sodium Hydrosulfite,
Na2S2O4)。亞硫酸鹽廣泛使用於脫水蔬菜、脫水水果、動物膠、糖蜜、糖飴、糖漬果實、蝦類、貝類、水果酒、澱粉等產品中,常見市售添加亞硫酸鹽的產
品則包括:金棗、鳳梨乾、脫水香蕉、葡萄乾、杏乾、柿餅、脫水金針、洋菇、筍乾、榨菜、綠豆芽、枸杞..等。
二氧化硫是酚氧化酉每的化學性抑制劑,同時也會與羰基化合物作用,所以當此類化合物存在時,必須加入過量之二氧化硫與其作用,方能將酚氧化酉每之活性去除
(張鈺驩,1990)。以二氧化硫抑制酚氧化酉每為一不可逆反應,將過量之二氧化硫去除時
(如:漂水過程),酚氧化酉每之活性亦無法恢復。但採用漂水過程時,應特別注意可溶性物質之流失,以免影響成品率。
產品內部若有空氣存在,少量之氧氣亦可造成褐變。因此,使用二氧化硫作為抑制劑時,必須考量二氧化硫之滲透。游離態 (自由態) 之二氧化硫
(Free Sulfite) 較亞硫酸鹽溶劑所形成之二氧化硫溶液更具有滲透性,亦可使用真空所產生之內外壓差將二氧化硫強制滲透進入產品內部。
二氧化硫易溶於水而生成H2SO3,且一旦與鹼作用則會轉變為SO32-、HSO3-、S2O52-。這些無機亞硫酸鹽離子在水溶液中會形成平衡狀態,其
個別存在之濃度則視pH值而定 (Green, 1976; Joslyn and Braverman, 1954)。其簡單化學變化方程式如下:

 pK1 = 2
pK1 = 2
 pK2 = 7
pK2 = 7
一般食品之pH範圍在3~7左右,大部份之亞硫酸鹽是以HSO3-狀態存在。唯有在很低之pH值下,SO2才會生成。pH值會影響食品內游離態與結合態
(Combined Sulfites)
之亞硫酸鹽之比例變化,游離態之亞硫酸鹽隨pH值降低而增加,若能控制pH值就可以控制食品內之亞硫酸鹽殘存量 (張炳揚,1988)。
亞硫酸鹽經氧化後會形成無毒之硫酸鹽,而在pH值小於4之食品,其所添加之亞硫酸鹽會以SO2形態揮發而散失,尤其是在加熱情況下。在許多食品中,僅有一小部份所添加之亞硫酸鹽是以游離態之無機亞硫酸鹽形態存在。
將亞硫酸鹽添加於食品中,其變化之情況係與食品之化學特性、加工方法與程度、儲存狀態與時間、包裝材料之滲透性及亞硫酸鹽之添加量等因素相關。亞硫酸鹽能
與食品中許多成份 (還原糖、醛類化合物、酮類化合物及蛋白質等)
進行穩定反應,而形成各種型式的結合態亞硫酸鹽。此外,在加工處理及貯存過程中,亞硫酸鹽非常容易與食品中其他成份產生反應,而形成各種亞硫酸鹽之有機化
合物,一旦亞硫酸鹽與其他有機成份結合後,就失去其特定作用,而使得亞硫酸鹽之用量隨產品種類而異。
二氧化硫在酸性情況下才會產生漂白及殺菌功效,其二氧化硫含量須在4,000 ppm以上才具有防腐效果
(洪美芳,1990)。二氧化硫濃度過低時,則無法抑制微生物生長;而當二氧化硫濃度過高時,則果膠質之分解速度加快,致使組織軟化,且具有刺激性氣味。
亞硫酸鹽殘留量明顯受到食品種類 (成份特性)、加工方法及貯存條件 (溫度、時間..等)
之影響,因此亞硫酸鹽在加工過程之用量與成品之殘留量亦非常難訂定一合理標準。一般蜜餞業者相信漂水過程可以大幅降低亞硫酸鹽殘留量,甚至完全除去亞硫酸
鹽。實際上,漂水過程僅能去除游離態之亞硫酸鹽 (Wedzicha, 1984)。
食品中添加之亞硫酸鹽因僅有一小部份是以游離態之無機亞硫酸鹽形態存在。以草莓果漿為例,所添加之亞硫酸鹽有98.5%
會在蒸煮過程中以SO2形態揮發,或是與果漿之成份反應結合,僅有少於1.5% 的游離態之無機亞硫酸鹽形態存在 (McWeeny et al.,
1980)。McBean (1967) 發現以亞硫酸鹽處理後之脫水水果中,絕大部份之二氧化硫在乾燥過程中已散失,而其餘80~90%
之亞硫酸鹽則以結合態存在,且在貯存過程中亞硫酸鹽亦會進一步散失。
一般針農採用偏重亞硫酸鈉 (Na2S2O5, 又稱焦亞硫酸氫鈉,Sodium Metabisulfite或Sodium
Pyro-bisulfite) 配製亞硫酸鹽溶液,其分子量為190,一分子之偏重亞硫酸鈉加水溶解後會游離產生兩個亞硫酸離子
(SO3-2)。因此,1% 濃度之偏重亞硫酸鈉若完全游離,僅能測得6,737-ppm之二氧化硫。亞硫酸氫鈉 (NaHSO3, Sodium
Bisulfite) 亦可用來配製亞硫酸鹽溶液,但其分子量為104,一分子之亞硫酸氫鈉加水溶解後僅能游離產生一個亞硫酸離子。因此,1%
濃度之亞硫酸氫鈉僅能測得6,154-ppm之二氧化硫。
聯合國糧農組織與世界衛生組織的食品添加物聯合專家委員會 (The Joint FAO/WHO Expert Committee on Food
Additives) 依據動物試驗結果,並設定100倍之安全係數估算,建議對亞硫酸鹽每日可接受攝取量 (ADI) 為0.7-mg/kg
body weight/day,故成人每日攝取容許量約為42-mg
(以60-kg體重計)。一般認為引起過敏性氣喘的因子是游離態之無機性亞硫酸鹽,而非結合態之有機性亞硫酸鹽,且無機性亞硫酸鹽之毒性較高。除非經常性
大量攝食,否則偶而超過每日攝取容許量亦不會對人體造成傷害。一般人食用亞硫酸鹽後,在體內亞硫酸鹽會轉變為硫酸鹽,然後隨著尿液排出體外,而通常成人每
日可經由尿液排出2.5-g之硫酸鹽。但是對於體內缺乏亞硫酸鹽氧化酵素 (Sulfite Oxidase)
的人而言,食用含有超量亞硫酸鹽的食物,因無法將亞硫酸鹽氧化成硫酸鹽而排出體外,可能會產生不同程度之過敏反應,引發哮喘與呼吸困難。在美國約有
0.05% 人口缺乏亞硫酸鹽氧化酵素,且以女性居多。因此美國食品藥物管理局 (FDA)
規定,食品二氧化硫殘留量在10-ppm以上者須明確標示註明,且禁止使用於生鮮蔬果 (例如:沙拉) 產品。
行政院衛生署於八十六年七月至十二月期間抽檢花東地區之金針生鮮與乾製品,檢驗結果顯示生鮮金針並未檢出二氧化硫殘留,但是乾製品部份計有84%檢測樣品
之二氧化硫殘留量超過500-ppm標準
(大部份檢測樣品在2,000-ppm以上,最高含量達20,300-ppm)。中華民國消費者文教基金會於八十七年九月出版之「消費者報導」報導金針乾
製品之二氧化硫殘留問題,消基會檢測之十四件市售金針乾製品皆超過500-ppm標準
(大部份檢測樣品在10,000~20,000-ppm,最高含量達30,000-ppm以上)。楊瑞森等 (1989)
檢測市售產品時發現金針乾製品及枸杞之二氧化硫殘留量分別為5,000-ppm及7,500-ppm,皆超過500-ppm標準。
金針乾製品復水浸泡處理
由於金針乾製品須經復水浸泡處理後方能進行烹調處理,而在復水浸泡過程中其含水率及二氧化硫殘留量有極大之變化。金針乾製品在復水浸泡過程中,其吸水量隨
浸泡溫度與時間增加而增加,而浸泡液之顏色逐漸變為黃色,顯示金針所含花青素類、黃色素類、胡蘿蔔素類等色素有溶出現象 (陳憶雯,1997)。
依據質量平衡原理,假設復水浸泡過程中二氧化硫未流失
(實際上二氧化硫會在復水浸泡過程中部份溶出而流失),而金針乾製品二氧化硫殘留量若為4,000-ppm,含水率為10%。經復水浸泡後其含水率增加至
90%,而二氧化硫殘留量則可降至 444-ppm。因此若考慮在復水浸泡過程中部份溶出之二氧化硫,則復水浸泡後金針之二氧化硫殘留量則可降至更低。
然而,在金針乾燥過程中其含水率及二氧化硫殘留量亦有極大之變化。生鮮金針含水率約為87~90%,而金針乾製品含水率約為8~20%。針農在進行金針加
工作業時,經常質疑為何以亞硫酸鹽浸泡後之金針二氧化硫殘留量僅1,000~2,000-ppm,但乾燥後其二氧化硫含量卻急遽升高。雖然二氧化硫會在金
針乾燥過程散失,且乾燥溫度越高,其散失量越多,但是乾燥過程中二氧化硫卻未隨水份蒸散流失。假設在金針乾燥過程中二氧化硫未流失,而浸泡亞硫酸鹽後之金
針二氧化硫殘留量為1,000-ppm,含水率為90%。經乾燥後其含水率降至10%,而二氧化硫殘留量則增加為9,000-ppm。若考慮乾燥過程中流
失之二氧化硫,則金針乾製品之二氧化硫殘留量會低於9,000-ppm。
金針經浸泡處理後可去除大部份之二氧化硫殘留量,相關之研究報告甚多。李善忱以市售金針乾製品 (二氧化硫含量為4,749-ppm)
浸泡30分鐘後,其二氧化硫殘留量可降至為500-ppm以下。徐錦豐等 (1994) 建議將金針乾製品浸於45℃ 溫水中至少20分鐘,或在25℃
冷水中至少60分鐘,可去除70% 之二氧化硫殘留量。陳憶雯 (1997) 分別針對高 (>10,000-ppm)、中
(1,500~10,000-ppm)、低 (<1,500-ppm) 二氧化硫殘留量之金針乾製品進行浸泡試驗,以25、80、100℃
溫度浸泡結果顯示,在30分鐘內中、低殘留量之金針乾製品皆可將二氧化硫殘留量降至500-ppm以下,但是高殘留量之金針乾製品則無法降至500-
ppm以下。林頎生和陳景川 (1989) 亦發現金針乾製品之二氧化硫殘留量過高時,浸泡處理仍無法有效降低二氧化硫殘留量。
目前部份農民為解決金針二氧化硫殘留量過高之問題,而將金針乾製品復水,再經漂水及乾燥過程以去除二氧化硫殘留量。雖然此法可確實去除二氧化硫殘留量至
500-ppm以下,金針顏色稍差。但如此不僅會增加加工成本,且在復水及漂水過程中因固形物之流失,而降低成品率,影響金針之口感與脆度。
文章定位: